日本で承認されている2つのAI医療機器についてまとめてみた!
こんにちは、加藤浩晃です。
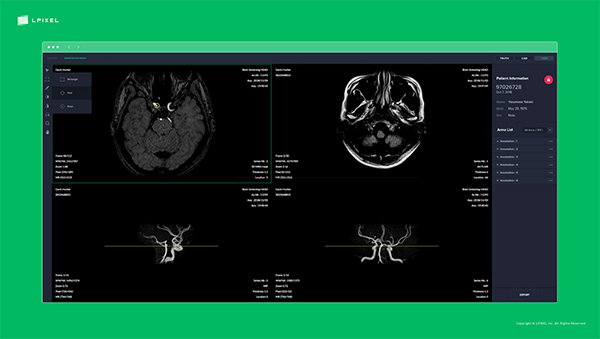
今日は各所から、国内2例目のAI医療機器として承認されたエルピクセル社の「医用画像解析ソフトウェア EIRL aneurysm(エイル アニュリズム)」についてめっちゃ質問をもらう一日でした・・。
それもこれも10月14日(月)に日経新聞で下記の記事が出たからなんですが、
そもそもこの「EIRL aneurysm(エイル アニュリズム)」って、9月17日に医療機器として承認されたもので、もう1か月前の話なんですよね・・・
ニュースで正確でない情報が出てきているし、明日以降問い合わせが来たら「ブログにまとめましたので、そちらを見てください!」って返事ができるように、『日本のAI医療機器の承認の現状』について話をまとめようと思います。
1.日本初のAI医療機器の承認
まずAI医療機器として日本で初めて承認がされたのは、記念すべき2018年12月6日で、サイバネットシステム株式会社の「内視鏡画像診断支援ソフトウェア EndoBRAIN」です。

医療機器にはリスクに応じて、リスクの低い「クラスⅠ」からリスクの高い「クラスⅣ」まで4段階に分類されているんですが、「EndoBRAIN」はクラスⅢです。
今までの医療機器の分類で当てはまるものがなかったので、新しく「疾患鑑別用内視鏡画像診断支援プログラム」という医療機器の分類(一般的名称)が新設されました。
ちょっとマニアックな話をすると、この画像診断支援プログラムは医療機器の国際分類GHTFルールで10-④の例外(b)“即座に危険となる臨床状態にある患者を診断するように意図した場合はクラスIIIである“に該当するとされたためクラスⅢとなっています。
「EndoBRAIN」は日本で初めて診断支援をするAI医療機器として承認がされ、医療機器の分類(一般的名称)も新設するという偉業を成し遂げているのです。
また、医療機器を販売するときには責任主体となる企業を決める必要があり、わかりにくい呼び方なのですが、その販売の責任者となる企業を「製造販売業」と言います。
「EndoBRAIN」の場合はサイバネットシステム株式会社が製造や、医療機器の承認の審査機関であるPMDAに申請をしているのですが、販売はオリンパスから行い、製造販売としての責任主体はオリンパスがするようなので、「オリンパスのEndoBRAIN」とも言われたりします。
(これもまた少しマニアックな話になるのですが、クラスⅢの医療機器の販売責任となろうとすると、第1種医療機器製造販売業という許可を受ける必要があります。クラスⅡだと第2種だけでよく、クラスⅠだけだと第3種製造販売業で可能です。)
ただ、承認まで頑張ったのは紛れもなくサイバネットシステム株式会社で、道なき道を切り開いて本当に偉大なことです。
2.今回のAI医療機器は国内初?2例目??
ここで、AI医療機器の2例目として今回のエルピクセル株式会社の「EIRL aneurysm(エイル アニュリズム)」なのですが、
「国内初」と書かれていたりすることもあるので、そこについて説明をしていきます。
AI医療機器として国内初は紛れもなく「EndoBRAIN」なのですが、実はEndoBRAINはAI開発で今よく聞く「ディープラーニング」で作っているわけではないんです。
EndoBRAINは「サポートベクターマシン」という手法(わからないとググってもらうほうがいいです)で作っているため、「ディープラーニング」ではないんです。
そのため「ディープラーニングで開発されたAI医療機器」として日本初なのはエルピクセルの「EIRL aneurysm」になります。
(ここら辺が結構ごちゃまぜに本日質問されたりしました・・)
ただ、今回のエルピクセル社の「EIRL aneurysm(エイル アニュリズム)」は医療機器の分類の大きな枠としては「MR装置ワークステーション用プログラム」というもので、EndoBRAINのような「〇〇画像診断支援プログラム」ではありません。
ではこのMR装置ワークステーションプログラムというのは何かと言うと、「MRIの画像を撮ったときに、わかりやすく画像を加工して表示するプログラム」です。
例えばMRIの画像のノイズ低減をしたり、fMRIだと脳の血液量や血流量など灌流分析して画面にカラーで表示ができたりする感じで、その脳画像を見る放射線科医や脳外科医によりわかりやくす表示してくれるんですね。
「MR装置ワークステーション用プログラム」は医療機器のリスク分類でいうとクラスⅡなので、普通はPMDAに承認申請するのではなく、PMDAが外部に委託した機関で医療機器を「認証」することで医療機器にすることができます。
クラスⅡの多くは医療機器を判断する際の基準(認証基準:3-888: 核医学装置ワークステーション用プログラム等基準)が決まっているため、それに合わせるだけでいいんです。
ただ、今回は通常のクラスⅡの医療機器に、AIでの脳動脈瘤の発見という+αが機能としてあるために、通常だと承認ではなく「認証」で済む医療機器の分類なのですが、「PMDAに承認申請」が必要なものになったのだと考えられます。
エルピクセルの製品としては、2018年10月16日に同じような汎用画像診断装置ワークステーション用プログラムとして「医用画像解析ソフトウェア EIRL basic」を出していますが、これはクラスⅡで他に特記すべき差がなかったのか「認証」で医療機器として認可されています。
3.まとめ
以上のことを今日は聞かれる一日だったので、このブログで整理をさせてもらいました。
(本当はもっとマニアックな話が色々とあるんですが、、、それは会ったときに話しましょう!!)
医療AIの研究開発が大学や企業で盛んになってきていて、いい成果も上がってきていますが、なかなか医療制度がわかりにくく医療現場で実際に使えるものとなるまでにハードルがあるのが現状です。
先行事例の情報を共有することで、どうやったら医療現場に届く医療機器となるのか多くの人に知ってもらえたらうれしいです!!
あと、まだ2つの医療機器とも保険適用とはなっていないので、「国内初の保険適用のAI医療機器」がどうなるかというのも引き続き楽しみにしています!!